
Představení produktu
| Fluorid hlinitý Základní informace |
| Popis Syntéza Aplikace Toxikologické studie Bezpečnost Reference |
| Název produktu: | Fluorid hlinitý |
| Synonyma: | fluoridhlinita;TRIFLUORID HLINÍKÝ;FLUORID HLINÍKÝ;Fluorid hlinitý;FLUORID HLINÍKÝ;FLUORID HLINÍKÝ;Fluorid hlinitý, 99.9+%,čistý;FLUORID HLINÍKU H |
| CAS: | 7784-18-1 |
| MF: | AlF3 |
| MW: | 83.98 |
| EINECS: | 232-051-1 |
| Kategorie produktů: | halogenid kovů; Anorganika; Anorganické fluoridy; Hliníkové soli; Hliník Nauka o kovech a keramice; Anorganika krystalické kvality; Věda o kovech a keramice; |
| Soubor Mol: | 7784-18-1.mol |
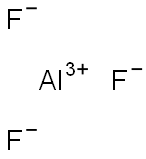 |
|
| Fluorid hlinitý Chemické vlastnosti |
| Bod tání | 1290 stupňů (lit.) |
| Bod varu | 1291 stupňů |
| hustota | 3,1 g/ml při 25 stupních (lit.) |
| Fp | 1250 stupňů |
| rozpustnost | Málo rozpustný v kyselinách a zásadách. Nerozpustný v acetonu. |
| formulář | prášek |
| barva | Bílá až světle šedá |
| Specifická gravitace | 2.882 |
| Rozpustnost ve vodě | MÍRNĚ ROZPUSTNÝ |
| Citlivý | Hygroskopický |
| Sublimace | 1250 ºC |
| Merck | 14,339 |
| Expoziční limity | ACGIH: TWA 2,5 mg/m3 NIOSH: IDLH 250 mg/m3; TWA 2 mg/m3; TWA 2,5 mg/m3 |
| Dielektrická konstanta | 2.2 (okolní) |
| Reference databáze CAS | 7784-18-1(Reference databáze CAS) |
| NIST Chemistry Reference | Fluorid hlinitý (7784-18-1) |
| Systém registru látek EPA | Fluorid hlinitý (7784-18-1) |
| Bezpečnostní informace |
| Kódy nebezpečí | Xn, T, Xi |
| Prohlášení o riziku | 22-36/37/38 |
| Bezpečnostní prohlášení | 26-37/39 |
| RIDADR | 3260 |
| WGK Německo | 1 |
| RTECS | BD0725000 |
| Poznámka k nebezpečí | Vysoce toxický/dráždivý |
| TSCA | Ano |
| Třída nebezpečnosti | 8 |
| PackingGroup | III |
| Kód HS | 28261210 |
| Údaje o nebezpečných látkách | 7784-18-1(Údaje o nebezpečných látkách) |
| Informace MSDS |
| Poskytovatel | Jazyk |
|---|---|
| Fluorid hlinitý | angličtina |
| SigmaAldrich | angličtina |
| ACROS | angličtina |
| ALFA | angličtina |
| Použití a syntéza fluoridu hlinitého |
| Popis | Fluorid hlinitý je ve formě bílé krystalické pevné látky nebo bílého prášku. Vyskytuje se přirozeně jako minerály rosenbergit a oskarssonit.1 Lze jej připravit i synteticky. |
| Syntéza | Fluorid hlinitý se vyrábí následujícími způsoby: 1) Kyselina fluorokřemičitá s hydroxidem hlinitým2 H2SiF6 + 2 Al(OH)3 → 2 AlF3 + SiO2 + 4 H2O (I) Reakce je exotermická a probíhá v několika krocích. To lze popsat následujícími třemi reakcemi: 3H2SiF6 + 2 Al(OH)3 → Al2(SiF6)3 + 6 H2O (II) Al2(SiF6)3 + 6 H2O → 2 AlF3 + 3 SiO2 + 12 HF (III) 12 HF + 4 Al(OH)3 → 4 AlF3 + 12 H2O Reakce se provádí mezi 70 °C a 100 °C. Koncentrace kyseliny fluorokřemičité může být až 35 % hmotn. ve vodném roztoku. Protože vyrobený roztok fluoridu hlinitého je metastabilní a trihydrát začíná rychle krystalizovat při teplotě kolem 90 °C, je nutné vysrážený pevný oxid křemičitý co nejrychleji odstranit. 2) Al2O3 s vodnou kyselinou fluorovodíkovou3 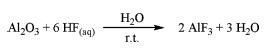 Do suspenze Al203 se za intenzivního míchání při teplotě místnosti přikape kyselina fluorovodíková. Následně se pevný oxid zcela rozpustí. Výsledný čirý roztok se míchá dny při teplotě místnosti. Během této doby se bílé pevné precipitáty oddělí od rozpouštědla, promyjí se vodou a následně se suší. Po zpracování v muflové peci při požadované kalcinační teplotě se získá fluorid hlinitý. 3) Alkoxid hlinitý s nevodným roztokem HF4 Alkoxid hlinitý, Al(OR)3 (R=Me, Et, iPr nebo tBu), reaguje s nevodným roztokem HF v organickém rozpouštědle. Reakce probíhá ve stavu sol-gel. Po stárnutí se vytvoří pevná látka, která se usadí. Pevná látka se oddělí centrifugací a suší se ve vakuu. Fluorace v plynné fázi vysušeného gelu se potom použije k získání fluoridu hlinitého. |
| Aplikace | Fluorid hlinitý je jednou z nejdůležitějších přísad v průmyslové výrobě hliníku. Použití fluoridu hlinitého může snížit bod tání kryolitu a zlepšit fyzikální a chemické vlastnosti elektrolytu. Při výrobě hliníku se oxid hlinitý rozpouští v roztoku kryolitu. Průchodem elektrického proudu roztokem vzniká hliník. Nicméně kryolitový roztok taje při asi 1000 stupních. Když se přidá fluorid hlinitý, může dojít k elektrolýze v kryolitovém roztoku při teplotě o 40-60 stupně nižší, čímž se sníží množství energie potřebné k výrobě hliníku.5 Fluorid hlinitý se používá jako bariérová vrstva ke zpomalení oxidace hliníkových zrcadel. 6 Používá se jako tavidlo do keramických glazur a emailů, při výrobě křemičitanu hlinitého a jako katalyzátor. Komplexy fluoridu hlinitého s proteiny lze použít ke studiu mechanistických aspektů reakcí přenosu fosforylů v biologii, které mají zásadní význam, protože anhydridy kyseliny fosforečné, jako je ATP a GTP, řídí většinu reakcí zapojených do metabolismu, růstu a diferenciace.8 Fluorid hlinitý se spolu s fluoridem zirkoničitým používá k výrobě fluorohlinitých skel. V zemědělství může být fluorid hlinitý použit k inhibici fermentace. Fyzikálně napařený fluorid hlinitý lze použít jako tenkou optickou vrstvu s nízkým indexem v situacích, kdy je vyžadována velká UV transparentnost.1 |
| Toxikologické studie | Perorální smrtelná dávka (LD5{1}}) fluoridu hlinitého pro zvířata je 0,1 g/kg. Fluorid hlinitý je méně toxický než většina fluoridů díky své nepatrné rozpustnosti ve vodě. Vystavení vysoké koncentraci fluoridu hlinitého způsobuje hypokalcémii. Vdechování a požití fluoridu hlinitého má za následek typické příznaky otravy fluoridem. Příznaky těžké otravy zahrnují dušnost, městnání plic, svalové křeče a křeče.8 Akutní (krátkodobé) toxické účinky mohou zahrnovat úhyn zvířat, ptáků nebo ryb a úhyn nebo nízkou rychlost růstu rostlin. Akutní účinky jsou pozorovány za 2 až 4 dny po expozici zvířat nebo rostlin fluoridu hlinitému. Chronické (dlouhodobé) toxické účinky mohou zahrnovat zkrácenou délku života, reprodukční problémy, nižší plodnost a změny vzhledu nebo chování u exponovaných zvířat. |
| Bezpečnost | Fluorid hlinitý je nehořlavá pevná látka. Je však nekompatibilní s mnoha dalšími komoditami včetně chemicky aktivních kovů (např. draslík a sodík), kyselinami a kyselými výpary. Kontakt může způsobit požár nebo výbuch. Při zahřívání se mohou uvolňovat toxické výpary fluoridu, včetně extrémně toxického fluorovodíku. |
| Reference |
https://en.wikipedia.org/wiki/Aluminium_fluorid John Karlström, model reaktoru pro výrobu fluoridu hlinitého W. Kleist, C. Häßner, O. Storcheva, K. Köhler, Jednoduchá syntéza fluoridu hlinitého s vysokým povrchem ve vodné fázi a jeho objemová a povrchová struktura, Inorganica Chimica Acta, 2006, sv. 359, str. 4851-4854 SK Ruediger, U. Groß, M. Feist, H A. Proscott, SC Shekar, SI Troyanov, E. Kemnitz, Nevodná syntéza mechanismu fluoridea hliníku s vysokým povrchem, Journal of Materials Chemistry, 2005, sv. 15, str. 588-597 https://info.noahtech.com R. Elaish, M. Curioni, K. Gowers, A. Kasuga, H. Habazaki, T. Hashimoto, P. Skeldon, Elelctrochimica Acta, 2017, sv. 245, str. 854-862 Alfred Wittinghofer, Signální mechanika: Fluorid hlinitý pro molekulu roku, 1997, sv. 7, str. R682-R685 Jeffrey Wayne Vincoli, Řízení rizik pro nebezpečné chemikálie, Bund 1, 1996, ISBN 1-56670-200-3 |
| Chemické vlastnosti | Fluorid hlinitý je bílý prášek nebo granule bez zápachu. |
| Chemické vlastnosti | Fluorid hlinitý, AlF3, je bezvodý krystalický prášek s bodem tání 1291 °C. Fluorid hlinitý (hydratovaný), AlF3·31/2H20 je bílý krystalický prášek, který je nerozpustný ve vodě. |
| Použití | Výroba hliníku pro snížení bodu tání a zvýšení vodivosti elektrolytu, tavidlo do keramických glazur a emailů, výroba křemičitanu hlinitého, katalyzátor. |
| Použití | Fluorid hlinitý se používá k výrobě hliníku s nízkou teplotou tání, jako tavidlo v keramických glazurách a bílých smaltech a jako katalyzátor při chemických reakcích. |
| Použití | V keramice, jako tavidlo v metalurgii, při výrobě hliníku, jako inhibitor kvašení, jako katalyzátor v organických reakcích Fluorid hlinitý se používá v procesu tavení ke snížení bodu tání elektrolytů, výroba křemičitanů hliníku, rafinace hliníkového odpadu, výroba speciálních výrobků žáruvzdorné výrobky a ve sklářském průmyslu jako plnivo. Používá se jako přísada tavidla k odstranění hořčíku. |
| Obecný popis | Bílý prášek nebo granule bez zápachu. Hustší než voda. Rozpustnost ve vodě při 25 stupních se rovná 0,559 g / 100 ml. |
| Reakce vzduchu a vody | Málo rozpustný ve vodě |
| Profil reaktivity | Fluorid hlinitý při zahřátí na sublimační podmínky uvolňuje toxické fluoridové výpary [USCG, 1999]. |
| Nebezpečí | Silně dráždí tkáň. |
| Zdravotní nebezpečí | AKUTNÍ: podráždění dýchacích cest; možné krvácení z nosu nebo zvracení; CHRONICKÁ: zhoršuje bronchitidu/astma; zvýšená hustota kostí. |
| Nebezpečí požáru | Zvláštní nebezpečí produktů spalování: Při zahřátí na sublimační podmínky uvolňuje toxické výpary fluoridu |
| Hořlavost a výbušnost | Nehořlavý |
| Bezpečnostní profil | Jed při požití. Středně toxický při subkutánním podání. Silně dráždí oči. Při kontaktu s Na a K prudce citlivý na náraz. Při zahřátí až do rozkladu uvolňuje toxické výpary F-. Viz také FLUORIDY a SLOUČENINY HLINÍKU. |
| Potenciální vystavení | Používá se jako součást elektrolytu, ze kterého se vyrábí kovový hliník; při výrobě keramiky, smaltů, křemičitanu hlinitého; jako tavidlo v metalurgii; jako inhibitor fermentace |
| Doprava | UN3260 Žíravá pevná látka, kyselá, anorganická, č., Třída nebezpečnosti: 8; Štítky: 8-Žíravý materiál, je vyžadován technický název. UN3077 Látky nebezpečné pro životní prostředí, pevné, č., Třída nebezpečnosti: 9; Štítky: 9-Různý nebezpečný materiál, je vyžadován technický název. |
| Nekompatibility | Prudce reaguje s draslíkem nebo sodíkem |
| Likvidace odpadu | Neutralizujte sodou; přidat hašené vápno; nechte stát 24 hodin. Převeďte kal do čistírny odpadních vod. |
| Produkty a suroviny na přípravu fluoridu hlinitého |
| Suroviny | Sulfuric acid-->Sodium carbonate-->Hydrogen fluoride-->Aluminum hydroxide-->Hexafluorosilicic acid-->Calcium fluoride-->PHOS ROCK FERTILIZER IN BULK-->Methylene Blue trihydrate-->Kyselina křemičitá |
| Přípravné produkty | Fluorohlinitan draselný |
Populární Tagy: fluorid hlinitý, Čína výrobci fluoridu hliníku, dodavatelé, továrna
Mohlo by se Vám také líbit
Odeslat dotaz


