
Představení produktu
| Kyselina fosforná Základní informace |
| Přehled Chemické vlastnosti Použití Toxicita IDENTIFIKACE NEBEZPEČNOSTI Způsob přípravy Způsob výroby |
| Název produktu: | Kyselina fosforná |
| Synonyma: | KYSELINA HYPOFOSFOREČNÁ,30%(W/V)SOLUTION;HYPOFOSOROUSACID,50%(W/V)SOLUTION;Kyselina hypofosforečná: (kyselina fosfinová);Kyselina hypofosforečná, 50%w/w aq. soln.;hypofosforná;hypofosforečná kyselina (žíravá kapalina,kyselá,anorganická,ne);kyselina hypofosforečná,50%w/waq.soln.;roztok KYSELINY HYPOFOSFOREČNÉ 50% VODNÝ |
| CAS: | 6303-21-5 |
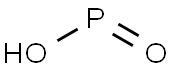
| MF: | HO2P |
| MW: | 63.980501 |
| EINECS: | 228-601-5 |
| Kategorie produktů: | HPA;Anorganika;6303-21-5 |
| Soubor Mol: | 6303-21-5.mol |
 |
|
| Kyselina fosforná Chemické vlastnosti |
| Bod tání | -25 stupeň |
| Bod varu | 108 stupňů (759,8513 mmHg) |
| hustota | 1,206 g/ml při 20 stupních (lit.) |
| tlak par | <17 mmHg ( 20 °C) |
| skladovací tepl. | žádná omezení. |
| rozpustnost | velmi rozpustný v H2O, ethanolu, ethyletheru |
| pka | pK1 1.1. |
| formulář | hygroskopické krystaly nebo bezbarvá olejovitá kapalina |
| barva | Bezbarvý |
| Rozpustnost ve vodě | ROZPUSTNÝ |
| Merck | 13,4894 |
| Stabilita: | Stabilní. Nekompatibilní se silnými bázemi. Prudce reaguje s oxidačními činidly, silnými zásadami, dusičnanem rtuťnatým (II) a oxidem rtuťnatým (II). Nezahřívejte nad 100 C. |
| InChIKey | GQZXNSPRSGFJLY-UHFFFAOYSA-N |
| Reference databáze CAS | 6303-21-5(Reference databáze CAS) |
| NIST Chemistry Reference | Kyselina fosforná (6303-21-5) |
| Systém registru látek EPA | Kyselina fosfinová (6303-21-5) |
| Bezpečnostní informace |
| Kódy nebezpečí | C |
| Prohlášení o riziku | 34 |
| Bezpečnostní prohlášení | 26-36/37/39-45 |
| RIDADR | OSN 3264 8/PG 3 |
| WGK Německo | 1 |
| RTECS | SZ6400000 |
| TSCA | Ano |
| Třída nebezpečnosti | 8 |
| PackingGroup | II |
| Kód HS | 28111990 |
| Údaje o nebezpečných látkách | 6303-21-5(Údaje o nebezpečných látkách) |
| Informace MSDS |
| Poskytovatel | Jazyk |
|---|---|
| Kyselina fosfinová | angličtina |
| SigmaAldrich | angličtina |
| ACROS | angličtina |
| ALFA | angličtina |
| Použití a syntéza kyseliny fosforné |
| Obrys | Kyselina fosforná je také známá jako "hypofosforitan" Je to bezbarvý olej nebo rozplývavý krystal, je to důležitý čistý chemický produkt. Hlavní použití je jako redukční činidlo pro bezproudové pokovování, fosfor zabraňující odbarvení pryskyřic, může být také použit v katalyzátoru esterifikační reakce, chladivu, zejména pro výrobu vysoce čistého produktu fosfornanu sodného. Existuje několik způsobů přípravy, běžným průmyslovým způsobem výroby je metoda iontoměničové pryskyřice a metoda elektrodialýzy. Chemické vlastnosti kyseliny fosforné, použití, toxicita a výrobní metody jsou upraveny andym z Chemicalbook. (2016-12-04) |
| Chemické vlastnosti | Jedná se o rozplývavé krystaly nebo bezbarvý olej. Teplota tání: 26,5 stupně. Relativní hustota (měrná hmotnost): 1,439 (pevná látka, 19 stupňů). Je rozpustný ve vodě, ethanolu a éteru a lze jej v libovolném poměru mísit s vodou, ethanolem, acetonem. Na vzduchu se snadno rozplývá na sirupovou kapalinu a vodný roztok je kyselý. Kyselina fosforná je jednosytná kyselina, ve vodném roztoku, kyselina fosforná je silná kyselina, Ka=10-2 (25 stupňů); je relativně stabilní při pokojové teplotě; disproporcionační reakce může probíhat při 130 stupních, rozkládat se na fosfin a kyselinu fosforitou: 2H3PO2=H3PO4+PH3 Má silnou redukci, roztok soli těžkých kovů lze obnovit na kovy, jako je Cu2 +, Hg2 +, Ag +, jako jsou: 4Ag+H3PO2+2H2)=4Ag+H3PO4+4H+ Je to slabé oxidační činidlo, může být redukováno na fosfin, fosfin, když se setká se silným redukčním činidlem. |
| Použití | 1. Kyselina fosforná se používá jako redukční činidlo pro bezproudové pokovování; 2. Může být použit k zabránění změny barvy pryskyřice kyseliny fosforečné; 3. Používá se jako esterifikační katalyzátor, chladivo; 4. Vyrábí se z něj fosfornan, soli sodné, soli manganu, soli železa se obecně používají jako výživné látky; 5. Kyselina fosforná se používá v lékařství a jako redukční činidlo, stanovení arsenu, teluru a separace tantalu, niobu a dalších činidel. 6. Je to silné redukční činidlo, lze jej použít pro přípravu fosfornanu sodného, fosforečnanu vápenatého a jiného fosfornanu. 7. Může být použit pro pokovovací lázeň. Léčiva. redukční činidlo. obecná činidla. 8. Je to silné redukční činidlo, lze jej použít při výrobě fosfornanu sodného, fosforečnanu vápenatého a jiného fosfornanu. 9. Tento produkt je široce používán jako redukční činidlo, Ag, Cu, Ni, Hg a další kovy jsou redukovány na odpovídající kov, pro ověření As, Nb, Ta a dalších činidel, lze jej použít pro přípravu Na , K, Ca, Mn, Fe a další typy fosfornanu. |
| Toxicita | Je nehořlavý. Ale při kontaktu s prostředkem otvoru H způsobí požár. Při setkání s oxidačním činidlem může probíhat prudká reakce a spalování. Když se zahřeje na vysokou úroveň, může se rozložit na vysoce toxický plynný fosfin nebo dokonce explodovat. Je žíravý. Kyselina fosforná se často přidává do nealkoholických nápojů, a protože se nevstřebává. Takže riziko je malé, ale zvláště silné hypofosforečnany poškozují gastrointestinální trakt. Náhodně vstříkne do očí nebo se dostane do kontaktu s pokožkou, k mytí se používá velké množství vody. Operátoři výroby by měli nosit ochranný oděv a jiné ochranné oděvy. Výrobní zařízení by mělo být utěsněno, dílna by měla být dobře větraná. |
| IDENTIFIKACE NEBEZPEČÍ | Prohlášení o nebezpečnosti: Způsobuje těžké poleptání kůže a poškození očí. Způsobuje vážné poškození očí Pokyny pro bezpečné zacházení: Nevdechujte prach/dým/plyn/mlhu/páry/aerosoly. Po manipulaci se důkladně umyjte. Používejte ochranné rukavice a ochranu očí/obličeje. PŘI POŽITÍ: Vypláchněte ústa. NEVYVOLÁVEJTE zvracení. PŘI STYKU S KŮŽÍ (nebo vlasy): Veškeré kontaminované oblečení okamžitě svlékněte. Opláchněte pokožku vodou/sprchou. PŘI ZASAŽENÍ OČÍ: Několik minut opatrně vyplachujte vodou. Vyjměte kontaktní čočky, pokud přítomný a snadno proveditelný. Pokračujte ve vyplachování. PŘI VDECHNUTÍ: Přeneste postiženého na čerstvý vzduch a ponechte jej v klidu v poloze usnadňující dýchání. Okamžitě volejte TOXIKOLOGICKÉ INFORMAČNÍ STŘEDISKO nebo lékaře. Obchod uzamčen. Zneškodněte tento materiál a jeho obal ve sběrně nebezpečného nebo speciálního odpadu. |
| Způsob přípravy | 1. Roztok fosforu a hydroxidu barnatého se zahřeje, může vzniknout barnatá sůl Ba (H2PO2) 2 • 2H2O, kyselina sírová se přidá do roztoku barya kyseliny fosforné, Ba2+ se může vysrážet: Ba(H2PO2)2+H2SO4=BaSO4+2H3PO2 Kyselinu fosfornou lze získat odpařením za sníženého tlaku a nízkoteplotní krystalizací. V důsledku tohoto procesu je rozpustnost baryové soli malá, takže koncentrace získané kyseliny fosforné není vysoká, průmyslový produkt by měl být čištěn rekrystalizací. 2. oxid barnatý (nebo vápno) a roztok bílého fosforu se společně zahřívají za vzniku sekundárního fosforečnanu barnatého (nebo vápníku) a poté reaguje s kyselinou sírovou, filtruje se, koncentruje se za získání produktu nebo postupuje roztok fosfornanu sodného H- iontoměničové pryskyřice typu mohou získat produkt. Tato metoda vyžaduje velké množství pryskyřice a krok regenerace pryskyřice a promývání je těžkopádný, obecně stojí více než 7 $ za libru, je vhodný pouze pro malosériovou výrobu a není vhodný pro průmyslové aplikace ve velkém měřítku. 3. Kyselina fosforná se připravuje metodou elektrodialýzy, kde se elektrodialyzační článek dělí na tři části, jsou to anodová komora, surovinová komora a katodová komora, meziprodukt je oddělen aniontovou membránou a kationtovou membránou, mezi dvě membrány je umístěn roztok fosfornanu sodného (koncentrace 100g/L~500g/L), anodová komora je zředěný roztok kyseliny fosforné 5g/L, anodová komora je zředěný roztok hydroxidu sodného (5g/L), mezi póly prochází DC (3V~36V), anoda uvolňuje kyslík a vytváří sekundární produkt kyseliny fosforné; katoda emituje vodík a vytváří sekundární produkt hydroxidu sodného, reakční doba je 3~21h. Reakce anodové komory a katodové komory jsou následující: anodová komora: H2O==H++OH- 2OH-==O2+2H2O+4e H++H2PO2-==H3PO2 katodová komora: H2O==H++OH- 2H++2e==H2 Na++OH-==NaOH Elektrodialyzační způsob přípravy Kyselina fosforná je jednoduchá a investice do zařízení malá, je vhodná pro hromadnou výrobu. 4. Počínaje průmyslově čistým fosfornanem sodným se anionty Cl-, SO{2}}, které ovlivňují ukazatele kvality kyseliny fosforné, odstraní srážením, ionty těžkých kovů se z roztoku odstraní vytvořením sulfidu a poté použitím silné kyseliny kationtoměničovou pryskyřici pro získání sekundárního fosforečnanu sodného, který lze získat jako produkt vysoké čistoty. Proces může produkovat vysoce kvalitní sekundární fosfát, technicky je proveditelný, proces je jednoduchý, snadný provoz, dobrá kvalita produktu, může splňovat potřeby elektronického průmyslu, obranného průmyslu a dalších high-tech oborů. 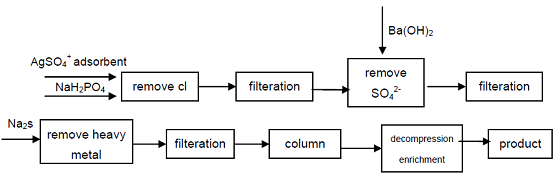 obrázek 1 Výrobní proces kyseliny fosforné z průmyslového fosfornanu sodného. 5. Metoda iontoměničové pryskyřice: asi 70 g kationtoměničové pryskyřice navlhčené vodou se naplní do skleněné zkumavky s 5 mol/l kyselinou chlorovodíkovou cirkulující asi 15 minut, po důkladném promytí vodou se získá vodný roztok fosfornanu sodného vysoké čistoty (15 g/ Protéká jím 60 ml H2O), sloupec pryskyřice se nejprve promyje 50 ml, poté 25 ml destilované vody. Odtékající kyselina a promývací kapalina se spojí, zahustí se odpařením ve vodní lázni. Koncentrovaná kyselina se umístí do vysokého vakua se sušičkou P205 za účelem dehydratace, chlazení a krystalizace, filtrace, rekrystalizace, čímž se získá produkt kyseliny fosforné. |
| Způsob výroby | Metoda iontoměničové pryskyřice: do skleněné zkumavky vložte asi 70 g ve vodě rozpustných katexových pryskyřic. Nechejte cirkulovat s 5 mol/l kyselinou chlorovodíkovou po dobu asi 15 minut a dostatečně promyjte vodou. Nechejte protéct kolonou pryskyřice vysoce vodný roztok fosfornanu sodného (15 g/60 ml H2O), poté promyjte nejprve 50 ml vody a poté opláchněte 25 ml destilované vody. Vytékající kyselina a promývací kapaliny byly spojeny a zakoncentrovány odpařením na vodní lázni. Koncentrovaná kyselina se posílá do vysoce vakuové sušárny P205 k dehydrataci, po které následuje ochlazovací krystalizace, filtrace a rekrystalizace za získání konečného produktu kyseliny fosforné. |
| Popis | Kyselina fosforná je silné redukční činidlo s molekulárním vzorcem H3PO2. Anorganičtí chemici označují volnou kyselinu tímto názvem, ačkoli její název IUPAC je dihydridohydroxidooxidophosphorus nebo přijatelný název kyseliny fosfinové. Je to bezbarvá sloučenina s nízkou teplotou tání, která je rozpustná ve vodě, dioxanu a alkoholech. Vzorec pro kyselinu fosfornou se obecně píše H3PO2, ale více popisným způsobem je HOP(O)H2, což zdůrazňuje její monoprotický charakter. Soli odvozené od této kyseliny se nazývají fosfináty (hypofosforitany). |
| Popis | Tato kyselina má obecný vzorec H4P2O6 a liší se od ostatních oxy-fosforových kyselin. Má mnoho zvláštností. Vzniká spolu s fosforem a kyselinami fosforečnými, když je fosfor oxidován vlhkým vzduchem. Pokud je bílý fosfor vystaven vzduchu a do kapaliny, která se tvoří, se přidá octan sodný, oddělí se poněkud nerozpustný fosforečnan sodný Na2H2P2O6·6H2O. Monohydrát hypofosforečnanu sodného je však velmi rozpustný a rozplývavý při -98,7 g/100 ml. |
| Chemické vlastnosti | bezbarvá kapalina |
| Fyzikální vlastnosti | Bezbarvé rozplývavé krystaly nebo olejovitá kapalina; kyselý zápach; hustota 1,493 g/cm3; taje při 26,5 stupni; vaří při 130 stupních; velmi rozpustný ve vodě, alkoholu a etheru; hustota 50% vodného roztoku je 1,13 g/ml. |
| Použití | Kyselina fosforná se primárně používá pro bezproudové pokovování niklem. Podílí se na redukci arenediazoniových solí. Působí jako přísada při Fischerových esterifikačních reakcích. Slouží také jako neutralizační činidlo, antioxidant, katalyzátor při polymeraci a polykondenzaci a smáčedlo. Dále se používá při formulaci léčiv, odbarvování polymerů, úpravě vody a získávání drahých nebo neželezných kovů. Kromě toho se používá jako bělidlo pro plasty, syntetická vlákna, odbarvovací prostředek a pro stabilizaci barvy při výrobě chemikálií a některých plastů. |
| Příprava | Kyselina fosforná se může připravit různými způsoby: 1. Vaření bílého fosforu s hydroxidem vápenatým: P4+ 4Ca(OH)2 + 8H2O → 4Ca(H2PO2)2 + 4H2 Vápenatá sůl je rozpustná ve vodě. Působením kyseliny sírové se získá kyselina hypofosforečná: (H2PO22Ca + H2TAK4 → 2H3PO2+ CaSO4 Směs produktu se filtruje, aby se odstranil nerozpustný CaS04. Vodný roztok kyseliny fosforné se zahustí za sníženého tlaku. Místo hydroxidu vápenatého lze použít koncentrovanou barytovou vodu.2. Zpracováním fosfornanu sodného, NaH2PO2 iontoměničovou pryskyřicí. Sodnou sůl lze vyrobit vařením bílého fosforu s roztokem hydroxidu sodného, což je reakce podobná (1) výše. PH3 + 2I2 + 2H2O → H3PO2+ 4Dobrý den, Výše uvedený způsob lze považovat za bezpečnější než způsob zahrnující zahřívání bílého fosforu s alkálií. Kyselina fosforná musí být skladována při teplotě do 50 stupňů. Komerčně se prodává jako vodný roztok v různých koncentracích. |
| Výrobní metody | Kyselina fosforná vzniká reakcí fosfornanu barnatého a kyseliny sírové a odfiltrováním síranu barnatého. Odpařením roztoku ve vakuu při 80 stupních a následným ochlazením na 0 stupňů krystalizuje kyselina fosforná. |
| Definice | ChEBI: Oxokyselina fosforu, která se skládá z jednoho pětimocného fosforu kovalentně vázaného jednoduchými vazbami na dva vodíky a hydroxyskupinu a přes dvojnou vazbu na kyslík. Rodič třídy fosfinových kyselin. |
| Definice | Bílá krystalická pevná látka. Je to jednosytná kyselina tvořící aniont H2PO2– ve vodě. Sodnou sůl, a tím i kyselinu, lze připravit zahříváním žlutého fosforu s roztokem hydroxidu sodného. Volná kyselina a její soli jsou silnými redukčními činidly. |
| Reakce | Kyselina fosforná je mísitelná s vodou ve všech poměrech a komerční síla je 30 % H3PO2. Fosfornany se používají v lékařství. Kyselina fosforná je silné redukční činidlo, např. se síranem měďnatým tvoří hydrid měďný Cu2H2, hnědou sraženinu, která uvolňuje plynný vodík a zahříváním zanechává měď; s dusičnanem stříbrným poskytuje jemně rozptýlené stříbro; s kyselinou sírovou poskytuje síru a trochu sirovodíku; s kyselinou sírovou poskytuje kyselinu siřičitou, která reaguje jako výše; vytváří mangan okamžitě s manganistanem. |
| Obecný popis | Kyselina fosforná se jeví jako bezbarvá olejovitá kapalina nebo rozplývavé krystaly s kyselým zápachem. Hustota 1,439 g / cm3. Teplota tání 26,5 stupně. Vdechování par dráždí nebo pálí dýchací cesty. Kapalina a páry mohou dráždit nebo pálit oči a pokožku. |
| Reakce vzduchu a vody | Rozplývající se. Rozpustný ve vodě. |
| Profil reaktivity | KYSELINA HYPOFOSFOROVÁ se zahříváním rozkládá na kyselinu fosforečnou a samovolně hořlavý fosfin. Oxiduje se kyselinou sírovou za uvolňování oxidu siřičitého a síry. Explozivně reaguje s oxidem rtuťnatým [Mellor, 1940, sv. 4, 778]. Prudce reaguje s dusičnanem rtuťnatým [Mellor, 1940, sv. 4, 993]. Neutralizuje báze při exotermických reakcích. |
| Nebezpečí | Nebezpečí požáru a výbuchu při kontaktu s oxidačními činidly. |
| Zdravotní nebezpečí | TOXICKÝ; vdechnutí, požití nebo kontakt s kůží s materiálem může způsobit vážné zranění nebo smrt. Kontakt s roztavenou látkou může způsobit vážné poleptání kůže a očí. Zabraňte jakémukoli kontaktu s pokožkou. Účinky kontaktu nebo vdechnutí mohou být opožděné. Oheň může vytvářet dráždivé, žíravé a/nebo toxické plyny. Odtok z požární nebo ředicí vody může být korozivní a/nebo toxický a způsobit znečištění. |
| Nebezpečí požáru | Nehořlavá látka sama o sobě nehoří, ale při zahřívání se může rozkládat a vytvářet korozivní a/nebo toxické výpary. Některé jsou okysličovadla a mohou zapálit hořlaviny (dřevo, papír, olej, oblečení atd.). Při kontaktu s kovy se může uvolňovat hořlavý plynný vodík. Nádoby mohou při zahřátí explodovat. |
| Způsoby čištění | Kyselina fosforitá je běžným kontaminantem komerční 50% kyseliny fosforné. Jenkins a Jones [J Am Chem Soc 74 1353 1952] tento materiál vyčistili odpařením asi 600 ml v 11 baňce při 40 °C za sníženého tlaku (v N2) na objem asi 300 ml. Poté, co byl roztok ochlazen, byl přenesen do Erlenmeyerovy baňky se širokým hrdlem, která byla uzavřena a ponechána v lázni suchý led/aceton po dobu několika hodin, aby zmrazila (v případě potřeby s poškrábáním stěny). Když pak byla baňka ponechána při cca 5 °C po dobu 12 hodin, asi 30-40 % zkapalnělo a bylo znovu přefiltrováno. Tento proces byl opakován, poté byla pevná látka uložena nad Mg(Cl04)2 ve vakuovém exsikátoru v chladu. Nezdálo se, že by následné krystalizace z n-butanolu jeho rozpuštěním při pokojové teplotě a poté ochlazením v lázni ledu a soli při -20o další čištění dále čistily. Volná kyselina tvoří rozplývavé krystaly m 26,5o a je rozpustná v H2O a EtOH. Sůl NaH2PO2 lze čistit pomocí aniontoměničové pryskyřice [Klement Z Anorg Allgem Chem 260 267 1949.] |
| Produkty a suroviny pro přípravu kyseliny fosforné |
| Suroviny | AMBERLITE(R) IRC-50 |
| Přípravné produkty | XANTHURENIC ACID-->3,5-diisopropylphenol-->cmtirust agent T-708-->Sodium hypophosphite-->TRIS(2,2'-BIPYRIDYL)RUTHENIUM(II) CHLORIDE HEXAHYDRATE-->4-IODOPYRIDINE-2-CARBOXYLIC ACID-->2,3,5,6-Tetrafluorophenol-->Benzothiazole, 4-methyl- (7CI,8CI,9CI)-->BEHENIC ACID METHYL ESTER-->Kyselina fosforitá |
Populární Tagy: kyselina fosforná, Čína výrobci kyseliny fosforné, dodavatelé, továrna
Dvojice: Bromičnan draselný
Další: Kyselina fluoroboritá
Mohlo by se Vám také líbit
Odeslat dotaz



