
Představení produktu
| Pyridin Základní informace |
| Chemická struktura Chemické vlastnosti Výroby Použití Informace o toxicitě Odkazy na nebezpečí |
| Jméno výrobku: | Pyridin |
| Synonyma: | pyridinkarboxylová kyselina,2-(4,5-dihydro-4-methyl-4-(1-methylethyl)-5-oxo-1h-imidazol{ {9}}yl)-5-methyl;pyridinkarboxylová kyselina,2-(4,5-dihydro-4-methyl-4-(1-methylethyl){{ 17}}oxo-1h-imidazol-2-yl)-5-methyl,monoamonná sůl;Rcra číslo odpadu U196;rcrawastenumberu196;FEMA 2932;FEMA 2966;FEMA ČÍSLO 2966;azabenzen |
| CAS: | 110-86-1 |
| MF: | C5H5N |
| MW: | 79.1 |
| EINECS: | 203-809-9 |
| Kategorie produktů: | Lahve z jantarového skla;NMR;Lahve na rozpouštědla;Rozpouštědlo podle aplikace;Rozpouštědlo podle typu;Možnosti balení rozpouštědel;Biotech SolventsRozpouštědla;Lahve na rozpouštědla;Rozpouštědla;Jistě/utěsnit? Láhve;Spektrofotometrická kvalita;Spektrofotometrická rozpouštědla;Rozpouštědla pro spektroskopii (IR;UV/Vis);Organostany;Tributylcín;Chemie;PS;Alpha Sort;Těkavé/polotěkavé látky;Lahve z jantarového skla;ReagentPlus(R) Solvent Slepe Products(R;ReagentPlus(R) Solvent Grade Products(R) ;ACS Grade Solvents;CHROMASOLV PlusCHROMASOLV Solvents (HPLC, LC-MS);CHROMASOLV(R) Plus;LC-MS Plus a Gradient;Abecední;P;PU - PZ;Pyridin;Organohalidy;Ester boron;Organoborony;Organosilan;ACS; -Velká rozpouštědla;Rozpouštědla třídy ACS;Kanystry z uhlíkové oceli se závity NPT;Rozpouštědla pro vratné nádoby;Rozpouštědla ACS a reagencie;ReagentPlus;ReagentPlus produkty v kvalitě rozpouštědel;Biotech rozpouštědla;Lahve s jistotou/těsněním;Stupeň ACS;Analytická analytická činidla pro všeobecné použití; ;Analytická/chromatografie;Multi-Compendial;Puriss pa;Puriss pa ACS;Lahve potažené PVC;Hliníkové lahve;CHROMASOLV Plus;Chromatografická činidla &;HPLC &;HPLC Plus Grade Solvents (CHROMASOLV);HPLC/UHPLCV rozpouštědla (CHULCHPOLV); Rozpouštědla (CHROMASOLV);Rozpouštědla třídy ACS;Kanystry z uhlíkové oceli se závity NPT;Poloobjemová rozpouštědla;Halogenované;Fluorované;Stavební bloky;Kyselina boritá;Karboxy;Alkoxy;Analytická činidla pro obecné použití;OP, Puriss pa;Puriss pa;OP , Puriss pa ACS;Puriss pa ACS;Hliníkové lahve;Abecední seznamy;Příchutě a vůně;OP;Spektrofotometrická rozpouštědla;Spektrofotometrická rozpouštědla;Lahve potažené PVC;ReagentPlus(R) Rozpouštědla };bc0001 |
| Soubor Mol: | 110-86-1.mol |
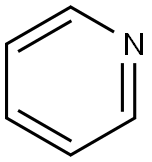 |
|
| Chemické vlastnosti pyridinu |
| Bod tání | -42 stupeň (rozsvícená) |
| Bod varu | 115 stupňů (lit.) |
| hustota | 0,978 g/ml při 25 stupních (lit.) |
| hustota páry | 2,72 (vs. vzduch) |
| tlak páry | 23,8 mm Hg (25 stupňů) |
| index lomu | n20/D 1,509 (lit.) |
| FEMA | 2966|PYRIDINE |
| Fp | 68 stupňů F |
| skladovací tepl. | Skladujte při +5 až +30 stupních. |
| rozpustnost | H2O: v souladu |
| pka | 5,25 (při 25 stupních) |
| formulář | Kapalina |
| barva | bezbarvý |
| Zápach | Nevolný zápach detekovatelný při 0,23 až 1,9 ppm (průměrně=0,66 ppm) |
| Relativní polarita | 0.302 |
| PH | 8,81 (H2O, 20 stupňů) |
| limit výbušnosti | 12.4% |
| Prahová hodnota zápachu | 0.063 str./min |
| Typ zápachu | rybí |
| Rozpustnost ve vodě | Mísitelný |
| Bod mrazu | -42 stupeň |
| λmax | λ: 305 nm Amax: 1.00 λ: 315 nm Amax: 0,15 λ: 335 nm Amax: 0,02 λ: {{0}} nm Amax: 0,01 |
| Merck | 14,7970 |
| BRN | 103233 |
| Konstanta Henryho zákona | 18,4 při 30 stupních (headspace-GC, Chaintreau et al., 1995) |
| Expoziční limity | TLV-TWA 5 ppm (-15 mg/m3(ACGIH, MSHA a OSHA); STEL 10 ppm (ACGIH), IDLH 3600 ppm (NIOSH). |
| Dielektrická konstanta | 12,5 (20 stupňů) |
| Stabilita: | Stabilní. Hořlavý. Nesnáší se se silnými oxidačními činidly, silnými kyselinami. |
| InChIKey | JUJWROOIHBZHMG-UHFFFAOYSA-N |
| LogP | 0.64 při 20 stupních |
| Reference databáze CAS | 110-86-1(Reference databáze CAS) |
| NIST Chemistry Reference | Pyridin (110-86-1) |
| IARC | 2B (sv. 77, 119) 2019 |
| Registrační systém látek EPA | Pyridin (110-86-1) |
| Bezpečná informace |
| Kódy nebezpečí | T, N, F, Xn |
| Prohlášení o riziku | 11-20/21/22-39/23/24/25-23/24/25-52-36/38 |
| Bezpečnostní prohlášení | 36/37/39-38-45-61-28A-26-28-24/25-22-36/37-16-7 |
| OEB | A |
| OEL | TWA: 5 ppm (15 mg/m3) |
| RIDADR | OSN 1282 3/PG 2 |
| WGK Německo | 2 |
| RTECS | 8400000 UR |
| F | 3-10 |
| Teplota samovznícení | 482 stupňů |
| Poznámka k nebezpečí | Vysoce hořlavý/Škodlivý |
| TSCA | Ano |
| HS kód | 2933 31 00 |
| Třída nebezpečnosti | 3 |
| Balící skupina | II |
| Údaje o nebezpečných látkách | 110-86-1(Údaje o nebezpečných látkách) |
| Toxicita | LD50 orálně u potkanů: 1,58 g/kg (Smyth) |
| IDLA | 1,000 str./min |
| Informace MSDS |
| Poskytovatel | Jazyk |
|---|---|
| SigmaAldrich | Angličtina |
| ACROS | Angličtina |
| ALFA | Angličtina |
| Použití a syntéza pyridinu |
| Chemická struktura | Pyridin je základní heterocyklická organická sloučenina s chemickým vzorcem C5H5N. Strukturálně je příbuzný benzenu, přičemž jedna methinová skupina (=CH−) je nahrazena atomem dusíku. Pyridinový kruh se vyskytuje v mnoha důležitých sloučeninách, včetně azinů a vitamínů niacinu a pyridoxinu.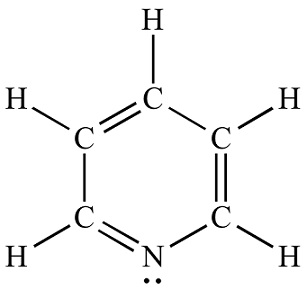 Struktura pyridinu Lewise |
| Chemické vlastnosti | Pyridin je bezbarvá hořlavá kapalina se silným a nepříjemným rybím zápachem. Pyridin |
| Produkce | 2.1 Oddělení od dehtu Pyridinové báze jsou složkou dehtů. Byly izolovány z uhelného dehtu nebo uhelného plynu před zavedením syntetických výrobních procesů. Množství obsažené v černouhelném dehtu a uhelném plynu je malé a z nich izolované pyridinové báze jsou směsí mnoha složek. Až na několik výjimek byla tedy izolace čistých pyridinových bází nákladná. Dnes se téměř všechny pyridinové báze vyrábějí syntézou.2.2 Syntéza chihibabinu 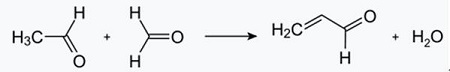 Obr. 2-1Tvorba akroleinu z acetaldehydu a formaldehydu 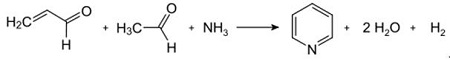 Obr. 2-2Kondenzace pyridinu z akroleinu a acetaldehydu Chichibabin pyridinová syntéza byla popsána v roce 1924 a stále se používá v průmyslu. Acetaldehyd a formaldehyd reagují s amoniakem za vzniku hlavně pyridinu. Nejprve se akrolein tvoří v Knoevenagelovu kondenzaci z acetaldehydu a formaldehydu. Poté se kondenzuje s acetaldehydem a amoniakem na dihydropyridin a poté se oxiduje katalyzátorem v pevném stavu na pyridin. Reakce se obvykle provádí při 350-550°C a prostorové rychlosti 500-1000h-1v přítomnosti pevného kyselého katalyzátoru (např. silika-alumina). Produkt se skládá ze směsi pyridinu, jednoduchých methylovaných pyridinů (pikolinu) a lutidinu. Izolovaný pyridin se oddělí od vedlejších produktů ve vícestupňovém procesu. 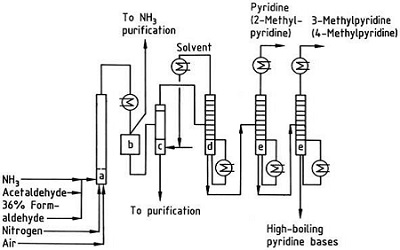 Obr. 2-3Schéma výroby pyridinu a methylpyridinu z acetaldehydu a formaldehydu s amoniakem. A) reaktor; b) Sběratel; c) extrakce; d) destilace rozpouštědla; e) Destilace 2.3 Dealkylace alkylpyridinů Pyridin lze připravit dealkylací alkylovaných pyridinů, které se získávají jako vedlejší produkty při syntézách jiných pyridinů. Oxidační dealkylace se provádí buď za použití katalyzátoru na vzduchu nad oxidem vanadičným, parní dealkylací na katalyzátoru na bázi niklu nebo hydrodealkylací s katalyzátorem na bázi stříbra nebo platiny. S katalyzátorem na bázi niklu lze dosáhnout výtěžků pyridinu až 93 %. 2.4 Syntéza z nitrilů a acetylenu Reakce nitrilů s acetylenem v kapalné fázi se provádí při 120-180 °C a 0.8-2,5 MPa v přítomnosti organokobaltového katalyzátoru a poskytuje 2-substituované pyridiny : 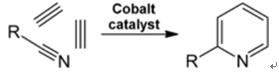 Obr. 2-4Syntéza 2-methylpyridinu z nitrilů a acetylenu Trimerizace části molekuly nitrilu a dvou částí acetylenu na pyridin se nazývá Bönnemannova cyklizace. Při použití acetonitrilu jako nitrilu se získá 2-methylpyridin, který lze dealkylovat na pyridin. 2.5 Syntéza z akrylonitrilu a ketonů 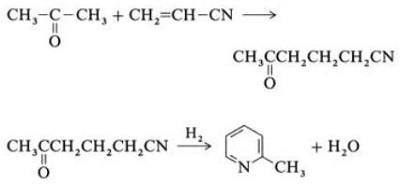 Obr. 2-5Syntéza 2-methylpyridinu z akrylonitrilu a acetonu Syntézou z akrylonitrilu a acetonu se selektivně získá 2-methylpyridin, který lze dealkylovat na pyridin. Za prvé, reakce akrylonitrilu a acetonu, katalyzovaná primárním alifatickým aminem, jako je isopropylamin, a slabou kyselinou, jako je kyselina benzoová, probíhá v kapalné fázi při 180 °C a 2,2 MPa za vzniku 5-oxohexannitrilu s 91 % selektivity. Konverze akrylonitrilu je 86 %. Poté se provádí cyklizace a dehydratace výchozího produktu v plynné fázi v přítomnosti vodíku na katalyzátoru obsahujícím palladium, nikl nebo kobalt při 240 °C za vzniku 2-methylpyridinu v 84% výtěžku. 2.6 Syntéza z dinitrilů Při reakci v plynné fázi nad katalyzátorem obsahujícím nikl v přítomnosti vodíku poskytuje 2-methylglutaronitril 3-methylpiperidin, který pak podléhá dehydrogenaci na palladiu a oxidu hlinitém za vzniku 3-methylpyridinu. A 3-methylpyridin lze také dealkylovat na pyridin. 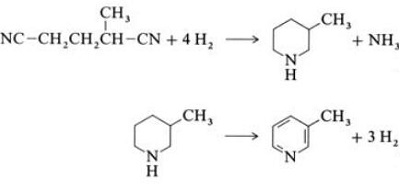 Obr. 2-6Syntéza 2-methylpyridinu z dinitrilů Uvádí se, že jednokroková reakce v plynné fázi na katalyzátoru obsahujícím palladium poskytuje 3-methylpyridin v 50% výtěžku. 2.7 Biosyntéza Několik pyridinových derivátů hraje důležitou roli v biologických systémech. Zatímco její biosyntéza není plně objasněna, kyselina nikotinová (vitamín B3) se vyskytuje u některých bakterií, hub a savců. Savci syntetizují kyselinu nikotinovou oxidací aminokyseliny tryptofan, kde meziprodukt, anilin, vytváří pyridinový derivát, kynurenin. Naopak bakterie Mycobacterium tuberculosis a Escherichia coli produkují kyselinu nikotinovou kondenzací glyceraldehyd 3-fosfátu a kyseliny asparagové. 2.8 Jiné metody Ethylen a amoniak reagují v přítomnosti katalyzátoru na bázi palladiového komplexu za vzniku 2-methylpyridinu a MEP. Pyridin lze připravit z cyklopentadienu ammoxidací nebo z 2-pentennitrilu cyklizací a dehydrogenací. Furfurylalkohol nebo furfural reaguje s amoniakem v plynné fázi za vzniku pyridinu. 2-Methylpyridin se také připravuje z anilinu. |
| Použití | 3.1 Rozpouštědlo Pyridin (110-86-1) je polární, bazické, málo reaktivní rozpouštědlo, zejména pro dehydrochlorační reakce a extrakci antibiotik. Při eliminační reakci působí pyridin jako báze eliminační reakce a váže výsledný halogenovodík za vzniku pyridiniové soli. Při esterifikacích a acylacích pyridin aktivuje halogenidy nebo anhydridy karboxylových kyselin. 3.2 Léky Chemickou strukturu pyridinu lze nalézt v různých lécích, které jsou syntetizovány částečně díky pyridinu. Jedním z příkladů je lék zvaný esomeprazol, obecný název pro Nexium. Toto je lék, který se používá k léčbě GERD nebo gastroezofageálního refluxu. Dalším příkladem léku obsahujícího pyridin je loratadin, běžněji známý pod obchodním názvem Claritin. Loratadin pomáhá při léčbě alergií. 3.3 Pesticidy Hlavní použití pyridinu je jako prekurzor herbicidů paraquat a diquat. První krok syntézy insekticidu chlorpyrifos sestává z chlorace pyridinu. Pyridin je také výchozí sloučeninou pro přípravu fungicidů na bázi pyrithionu. Cetylpyridinium a laurylpyridinium, které lze vyrobit z pyridinu Zinckeho reakcí, se používají jako antiseptikum v přípravcích pro ústní a zubní péči. Pyridin je snadno atakován alkylačními činidly za vzniku N-alkylpyridiniových solí. Jedním příkladem je cetylpyridiniumchlorid.  Obr 3-1 Syntéza parakvatu 3.4 Syntéza piperidinu Piperidin, základní dusíkatý heterocyklus, je důležitým syntetickým stavebním kamenem. Piperidiny se vyrábějí hydrogenací pyridinu s katalyzátorem na bázi niklu, kobaltu nebo ruthenia při zvýšených teplotách. C5H5N + 3 H2 → C5H10NH3,5 Ligand a Lewisova báze Pyridin je široce používán jako ligand v koordinační chemii. Jako ligand kovového komplexu jej lze snadno nahradit silnější Lewisovou bází, kterou lze využít při katalýze polymeračních a hydrogenačních reakcí. Po dokončení reakce může být pyridinový ligand nahrazený během reakce znovu obnoven. Pyridin se také používá jako báze při kondenzačních reakcích. Jako základ lze jako Karl Fischerovo činidlo použít pyridin, ale obvykle je nahrazen alternativami s příjemnější vůní, jako je imidazol. 3.6 Ostatní Kromě výše uvedených použití se Pyridin také používá k výrobě polykarbonátových pryskyřic, vitamínů, potravinářských příchutí, barev, barviv, pryžových výrobků, lepidel a hydroizolací pro tkaniny. Pyridin se přidává do ethanolu, aby byl nevhodný k pití. Používá se také při syntéze DNA in vitro. |
| Informace o toxicitě | 4.1 Úroveň toxicity Nízká toxicita 4.2 Akutní toxicita LD501580 mg/kg (velké myši, orálně); 1121 mg/kg (králík, přes kůži); inhalováno člověkem 25mg/m3×20 min, podráždění spojivek a sliznice horních cest dýchacích. Subakutní a chronická toxicita: inhalované velkými myšmi 32,3 mg/m3×7 hodin/den x5 dní/týden x6 měsíců, zvýšení hmotnosti jater; vdechované lidmi 20-40mg/m3 (dlouhodobě), poškození nervů, nestabilní chůze, digitální třes, nízký krevní tlak, nadměrné pocení, občasné poškození jater a ledvin. |
| Rizika | 5.1 Nebezpečí pro zdraví Pyridin je extrémně toxický při požití a vdechování. Páry jsou těžší než vzduch. jeho spalováním vznikají toxické oxidy dusíku. Pyridin je vysoce hořlavý (bod vzplanutí je pouze 17 ºC). Pyridin může mít také neurotoxické a genotoxické účinky. 5.2 Nebezpečí požáru Chování při požáru: Páry jsou těžší než vzduch a mohou urazit značnou vzdálenost ke zdroji vznícení a vzplanout. |
| Reference |
https://cs.wikipedia.org/wiki/Pyridine#Occurrence http://www.zwbk.org/MyLemmaShow.aspx?zh=zh-tw&lid=169038 http://www.softschools.com/formulas/chemistry/pyridine{0}}vzorec/378/ http://www.hmdb.ca/metabolites/HMDB0000926 https://study.com/academy/lesson/pyridine-in-medicine-uses-synthesis.html#partialRegFormModal http://www.toxipedia.org/display/toxipedia/Pyridine https://www.chemicalbook.com/ProductChemicalPropertiesCB8852825_CS.htm https://pubchem.ncbi.nlm.nih.gov/compound/pyridine#section=Nahoru http://www.ebi.ac.uk/chebi/searchId.do;jsessionid=E7088896622D62FC650863C2AD197CAA?chebiId=CHEBI:16227 https://www.britannica.com/science/pyridine Shimizu, S.; Watanabe, N.; Kataoka, T.; Shoji, T.; Abe, N.; Morishita, S.; Ichimura, H. (2005), "Pyridine and Pyridine Derivatives", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_399 |
| Chemické vlastnosti | Pyridin, je slabě žlutá nebo bezbarvá kapalina; hygroskopický; nepříjemný zápach; pálivá chuť; mírně alkalický v reakci; rozpustný ve vodě, alkoholu, etheru, benzenu a mastných olejích; specifická hmotnost, 0.978; teplota samovznícení, 482 stupňů. Pyridin, terciární amin, je poněkud silnější báze než anilin a snadno tvoří kvartérní amoniové soli. |
| Chemické vlastnosti | Pyridin je slabá báze (pKa{{0}}.25); 0,2 M roztok má pH 8,5 (HSDB 1988). Jeho uhlíkové atomy jsou deaktivovány směrem k elektrofilní substituci. To platí zejména v kyselém prostředí, kde se na dusíku tvoří soli. Snadno však podléhá nukleofilní substituci, přednostně v poloze C-2 a také v poloze C-4 (Jori et al 1983). Jako terciární amin reaguje pyridin s alkylačními činidly za vzniku kvartérních solí (Santodonato et al 1985). Vzhledem ke své snížené schopnosti darovat elektrony je odolnější vůči oxidaci než benzen. Oxidací peroxykyselinami vzniká pyridin N-oxid, který je poté schopen elektrofilní substituce (Jori et al 1983). Pyridin prudce reaguje s řadou sloučenin, včetně kyseliny dusičné, kyseliny sírové, anhydridu kyseliny maleinové, perchromátu, beta-propiolaktonu a kyseliny chlorsulfonové. Tepelný rozklad může uvolnit kyanidy (Gehring 1983). Jak pyridiniový iont, tak samotný pyridin se snadno redukují na komerčně důležitou sloučeninu, piperidin (Jori a kol. 1983). |
| Fyzikální vlastnosti | Čirá, bezbarvá až světle žlutá, hořlavá kapalina s ostrým, pronikavým, nechutným rybím zápachem. Prahové koncentrace zápachu ve vodě a vzduchu byly 2 ppm (Buttery et al., 1988) a 21 ppbv(Leonardos et al., 1969), resp. Detekční prahové koncentrace pachu 0,74 mg/m3(2,3 ppmv) a 6 mg/m3(1,9 ppmv) byly experimentálně stanoveny Katzem a Talbertem (1930) a Dravnieksem (1974). Cometto-Mu?iz a Cain (1990) uvedli průměrnou prahovou koncentraci štiplavosti v nosu 1 275 ppmv. |
| Výskyt | Pyridin objevil Anderson v černouhelném dehtu v roce 1846 (Windholz et al 1983). Nachází se v tabákovém kouři (Vohl a Eulenberg 1871; Lehmann 1909) a pražené kávě (Bertrand a Weisweiller 1913). Pyridin se nachází v oleji ze dřeva a v listech a kořenech Atropa belladonna (HSDB 1988) a je také součástí kreosotového oleje (Krone et al 1986). V přírodě se pyridin a jeho deriváty běžně vyskytují jako složky alkaloidů, vitamínů a koenzymů. |
| Použití | Pyridin se používá jako rozpouštědlo v průmyslu barev a gumy; jako meziprodukt v barvivech a léčivech; pro denaturaci alkoholu a jako činidlo pro analýzu kyanidu. Vyskytuje se v černouhelném dehtu. |
| Použití | Pyridin se používá přímo při denaturaci alkoholu (ACGIH 1986; HSDB 1989; NSC 1978) a jako rozpouštědlo při přípravě barev a pryže (ACGIH 1986; HSDB 1989; NSC 1978) a ve výzkumných laboratořích pro funkce, jako je extrakce rostlinných hormonů ( Santodonato a kol. Polovina dnes vyráběného pyridinu se používá jako meziprodukt při výrobě různých insekticidů a herbicidů pro zemědělské aplikace (ACGIH 1986; Harper a kol. 1985; Santodonato a kol. 1985). Přibližně 20 % jde do výroby piperidinu (Harper a kol. 1985; Santodonato a kol. 1985), který je komerčně významný při přípravě chemikálií používaných při vulkanizaci pryže a zemědělství (NSC 1978). Pyridin se také používá jako meziprodukt při přípravě léčiv (antihistaminika, steroidy, sulfa-typ a další antibakteriální činidla), barviv, vodoodpudivých látek a polykarbonátových pryskyřic (ACGIH 1986; Harper a kol. 1985; NSC 1978; Santodonato a kol. 1985). Pyridin je také schválen Food and Drug Administration (FDA) pro použití jako ochucovadlo při přípravě potravin (Harper et al. 1985; HSDB 1989). |
| Definice | ChEBI: Pyridin je azaaren obsahující benzenové jádro, ve kterém je jedna skupina -CH nahrazena atomem dusíku. Je to mateřská sloučenina třídy pyridinů. Molekuly mají šestiúhelníkový rovinný kruh a jsou isoelektronické s benzenem. Pyridin je příkladem aromatické heterocyklické sloučeniny s elektrony ve vazbách uhlík-uhlík pi a osamoceným párem dusíku delokalizovaným přes kruh atomů. Sloučenina se extrahuje z černouhelného dehtu a používá se jako rozpouštědlo a jako surovina pro organickou syntézu. |
| Výrobní metody | Pyridin se vyrábí z plynů získaných koksováním uhlí a přímou syntézou. Frakce lehkého oleje černouhelného dehtu se zpracovává kyselinou sírovou za vzniku ve vodě rozpustných pyridinových solí a poté se pyridinové báze izolují z vodné fáze hydroxidem sodným nebo amoniakem (Jori et al 1983). Většina americké produkce se vyrábí syntetickými prostředky. Tento proces využívá reakci acetaldehydu, formaldehydu a amoniaku v parní fázi, která poskytuje směs pyridinu a 3-methylpyridinu (Santodonato et al 1985). Poměr produktů závisí na relativních množstvích acetaldehydu a formaldehydu. Přidaný methanol zvyšuje výtěžek. Produkce pyridinu v USA byla v roce 1975 odhadována na 32 až 47 milionů liber (Reinhardt a Brittelli 1981). Pyridin je komerčně dostupný v technických, 2stupňových a 1stupňových třídách, přičemž poslední dva se vztahují k jejich rozmezím varu. Hlavními nečistotami jsou homology s vyšší teplotou varu, jako jsou pikoliny, lutidiny a kollidiny, což jsou mono-, di- a trimethylpyridiny (Santodonato et al 1985; Jori et al 1983). |
| Příprava | Pyridin se vyrábí buď izolací z přírodních zdrojů, jako je uhlí, nebo chemickou syntézou (HSDB 1989). Pyridin se vyrábí frakční destilací uhelných dehtových zbytků (HSDB 1989; NSC 1978; Santodonato et al. 1985), při níž 1 tuna uhlí produkuje 0.07-0,21 liber pyridinových bází z nichž 57 % je pyridin (Santodonato et al, 1985). Synteticky vyráběný pyridin je v současnosti důležitějším zdrojem pyridinu pro komerční použití (Santodonato et al. 1985). Malá množství pyridinu se syntetizují z acetaldehydu, formaldehydu a amoniaku s fluidizovaným oxidem křemičitým-aluminovým katalyzátorem, po kterém následuje frakcionace za účelem izolace pyridinu (Harper et al. 1985; HSDB 1989; NSC 1978). Pyridin je produkován z přírodních zdrojů společností Crowley Tar Products of Stow, Ohio a Oklahoma City, Oklahoma (Harper a kol. 1985; HSDB 1989; SRI 1986, 1987, 1988). Pyridin je synteticky vyráběn dvěma společnostmi, Nepera Chemical Co. z Harriman, New York a Reilly Tar and Chemical Corporation z Indianapolis, Indiana (Harper a kol. 1985; SRI 1986, 1987, 1988). |
| Prahové hodnoty aroma | Detekce: 0.079 až 790 ppb; rozpoznávání: 7,9 až 40 ppm |
| Obecný popis | Čirá bezbarvá až světle žlutá kapalina s pronikavým zápachem na zvracení. Hustota 0,978 g/cm3. Bod vzplanutí 68 stupňů F. Páry jsou těžší než vzduch. Toxický při požití a vdechování. Spalováním vznikají toxické oxidy dusíku. |
| Reakce vzduchu a vody | Vysoce hořlavý. Rozpustný ve vodě. |
| Profil reaktivity | Azabenzen je báze. S kyselinami reaguje exotermicky. Při přípravě komplexu azabenzenu s oxidem chromovým, kyselinou, došlo ke zvýšení podílu oxidu chromitého. Zahřívání z této acidobazické reakce vedlo k explozi a požáru [MCA Case History 1284 1967]. 0,1% roztok azabenzenu (nebo jiného terciárního aminu) v maleinanhydridu při 185 stupních poskytuje exotermický rozklad s rychlým vývojem plynu [Chem Eng. Zprávy 42(8); 41 1964]. Míchání azabenzenu ve stejných molárních dávkách s některou z následujících látek v uzavřené nádobě způsobilo zvýšení teploty a tlaku: kyselina chlorsulfonová, kyselina dusičná (70 %), oleum, kyselina sírová (96 %) nebo propiolakton [NFPA 1991]. Kombinace jódu, azabenzenu, oxidu sírového a formamidu vytvořila po několika měsících přetlakování plynu. To vzniklo z pomalé tvorby kyseliny sírové z vnější vody nebo z dehydratace formamidu na kyanovodík. Ethylenoxid a SO2 mohou prudce reagovat v roztoku azabenzenu s natlakováním, pokud je ethylenoxidu přebytek (Nolan, 1983, Case History 51). |
| Nebezpečí | Hořlavost, nebezpečí požáru, limity výbušnosti ve vzduchu 1,8–12,4 %. Toxický při požití a vdechování. Dráždí kůži, poškození jater a ledvin. Pochybný karcinogen. |
| Hazardování se zdravím | Akutní toxicita pyridinu je nízká. Inhalace způsobuje podráždění dýchacího systému a může ovlivnit centrální nervový systém, což způsobuje bolest hlavy, nevolnost, zvracení, závratě a nervozitu. Pyridin dráždí oči a kůži a snadno se vstřebává, což vede k systémovým účinkům. Požití pyridinu může způsobit poškození jater a ledvin. Pyridin způsobuje čichovou únavu a jeho zápach neposkytuje dostatečné varování před přítomností škodlivých koncentrací. Nebylo zjištěno, že by pyridin byl karcinogenní nebo vykazoval reprodukční nebo vývojovou toxicitu u lidí. Chronická expozice pyridinu může vést k poškození jater, ledvin a centrálního nervového systému. |
| Hazardování se zdravím | Toxické účinky pyridinu zahrnují bolest hlavy, závratě, nervozitu, nevolnost, nespavost, časté močení a bolesti břicha. Příznaky byly přechodné, objevily se u lidí ze subakutní expozice pyridinovým výparům při asi 125 ppm po dobu 4 hodin denně po dobu 1–2 týdnů (Reinhardt a Brittelli 1981). Cílovými orgány pro toxicitu pyridinu jsou centrální nervový systém, játra, ledviny, gastrointestinální trakt a kůže. Cesty expozice jsou vdechování par a požití a absorpce kapaliny kůží. Vážná zdravotní rizika mohou vzniknout v důsledku chronického vdechování, které může způsobit poškození ledvin a jater, a stimulace kostní dřeně ke zvýšení tvorby krevních destiček. Nízká expozice 10 ppm může vyvolat chronické otravy na centrální nervový systém. Požití kapaliny může vyvolat stejné příznaky, jaké jsou uvedeny výše. Kontakt s kůží může způsobit dermatitidu. Pára dráždí oči, nos a plíce. Kvůli jeho silnému nepříjemnému zápachu je vždy dostatečné varování před jakýmkoli přeexponováním. Koncentrace 10 ppm je pro člověka nežádoucí. Hodnota LCLO, inhalace (krysy): 4000 ppm/4 h Hodnota LD50, orálně (myši): 1500 mg/kg. Huh a spolupracovníci (1986) zkoumali účinek kyseliny glycyrrhetinové na toxicitu pyridinu u myší. Předběžná léčba kyselinou glycyrrhetinovou snížila depresi centrálního nervového systému a mortalitu u zvířat vyvolanou pyridinem. Taková předléčení výrazně snížilo aktivitu enzymu sérové transaminázy a zvýšilo aktivitu jaterní mikrosomální anilinhydroxylázy [9012-90-0], enzymu metabolizujícího pyridin. |
| Hořlavost a výbušnost | Pyridin je vysoce hořlavá kapalina (hodnocení NFPA=3) a jeho páry mohou urazit značnou vzdálenost a „vzplanout zpět“. Páry pyridinu tvoří se vzduchem výbušné směsi v koncentracích 1,8 až 12,4 % (obj.). Při požárech pyridinu by se měl používat oxid uhličitý nebo suché chemické hasicí přístroje. |
| Průmyslové využití | Pyridin je dobrým rozpouštědlem pro velké množství sloučenin, organických i anorganických (Windholz et al 1983). Asi 50 % pyridinu používaného v USA je pro výrobu zemědělských chemikálií, jako jsou herbicidy paraquat, diquat a triclopyr a insekticid chlorpyrifos. Další použití jsou při výrobě piperidinu; výroba léčiv, jako jsou steroidy, vitamíny a antihistaminika; a jako rozpouštědlo. Použití rozpouštědel se nachází jak ve farmaceutickém průmyslu, tak ve výrobě polykarbonátových pryskyřic. Je zvláště užitečný jako rozpouštědlo v procesech, kde se vyvíjí HC1 (Santodonato et al 1985). V menší míře se pyridin používá pro denaturaci alkoholu a nemrznoucích směsí, jako pomocný prostředek při barvení textilií a jako ochucovadlo (Jori a kol. 1983; Furia 1968; HSDB 1988). |
| Kontaktní alergeny | Pyridin (nesubstituovaný pyridin) a jeho derivát (substituované pyridiny) jsou široce používány v chemii. Pyridin je rozpouštědlo používané pro mnoho organických sloučenin a chemikálií bezvodých kovových solí. Obsažený v Karl Fischerově činidle vyvolal u laboratorního technika kontaktní dermatitidu. Mezi těmito různými látkami nebyla pozorována žádná zkřížená citlivost. |
| Bezpečnostní profil | Jed intraperitoneální cestou. Středně toxický při požití, styku s kůží, intravenózním a subkutánním podáním. Mírně toxický při vdechování. Silně dráždí kůži a oči. Údaje o mutaci hlášeny. Může způsobit depresi centrálního nervového systému, gastrointestinální potíže a poškození jater a ledvin. Hořlavá kapalina a nebezpečí požáru při vystavení teplu, plameni nebo oxidantům. Vážné nebezpečí výbuchu ve formě páry při vystavení plameni nebo jiskrám. Prudce reaguje s kyselinou chlorsulfonovou, oxidem chromovým, oxidem dusnatým, HNO3, oleem, perchromáty, ppropiolaktonem, AgClO4, H2SO4. Reakce žárovky s fluorem. Reaguje za vzniku samozápalných nebo výbušných produktů s fluoridem bromitým, trifluormethyl hypofluoritem. Směsi s formamidem + jodem + oxidem sírovým jsou nebezpečné při skladování, uvolňují oxid uhličitý a kyselinu sírovou. Nesnáší se s oxidačními materiály. Reaguje s anhydridem kyseliny maleinové (nad 150 stupňů) a uvolňuje oxid uhličitý. K hašení ohně použijte alkoholovou pěnu. Při zahřátí na rozklad uvolňuje vysoce toxické výpary NOx. |
| Potenciální vystavení | Pyridin se používá jako rozpouštědlo v chemickém průmyslu a jako denaturační činidlo pro ethylalkohol; jako meziprodukt při výrobě pesticidů; ve farmacii; při výrobě barev, výbušnin, barviv, kaučuku, vitamínů, sulfátových léčiv; a dezinfekční prostředky. |
| Karcinogenita | V několika chronických subkutánních studiích nebyl pyridin karcinogenní. Krysám F344 byl podáván pyridin orálně v pitné vodě v dávkách 0, 7, 14 nebo 33 mg/kg po dobu 2 let. Nejvyšší dávka způsobila snížení tělesné hmotnosti a spotřeby vody. Zvýšený renální tubulární adenom nebo karcinom a tubulární hyperplazie byly pozorovány u mužů při dávce 33 mg/kg. Zvýšená leukémie mononukleárních buněk byla pozorována u samic při dávkách 14 a 33 mg/kg, což bylo považováno za nejednoznačné z hlediska vztahu k expozici pyridinu, protože jde o běžný nález u tohoto kmene potkanů. Nenádorové změny v játrech související s koncentrací byly pozorovány při dávce 33 mg/kg. Samci potkanů Wistar byli podobně léčeni dávkami 0, 8, 17 nebo 36 mg/kg po dobu 2 let. Snížení přežití a tělesné hmotnosti bylo pozorováno při 17 a 36 mg/kg. Zvýšené adenomy testikulárních buněk byly pozorovány při dávce 36 mg/kg. Nebyly hlášeny žádné změny v přežití nebo výskytu novotvarů v jiných tkáních, včetně ledvin, ačkoli u některých potkanů léčených pyridinem byla pozorována zvýšená nefropatie a jaterní centrilobulární degenerace/nekróza. |
| Zdroj | Pyridin se přirozeně vyskytuje v bramborách, anabázi, listech kurníku, mátě peprné (0 až 1 ppb), čajových listech a listech tabáku (Duke, 1992). Identifikována jako jedna ze 140 těkavých složek v použitých sójových olejích odebraných ze zpracovatelského závodu, který smažil různé produkty z hovězího, kuřecího a telecího masa (Takeoka et al., 1996). |
| Environmentální osud | Biologický.Heukelekian a Rand (1955) uvedli hodnotu 5-d BSK 1,31 g/g, což je 58,7 % hodnoty ThOD 2,23 g/g. A Nocardia sp. izolovaný z půdy byl schopen přeměnit pyridin v přítomnosti semikarbazidu na meziprodukt identifikovaný jako semialdehyd kyseliny jantarové (Shukla a Kaul, 1986). 1,4-Dihydropyridin, dialdehyd glutarové, semialdehyd kyseliny glutarové a kyselina glutarová byly identifikovány jako meziprodukty při degradaci pyridinu kmenem Nocardia Z1 (Watson a Cain, 1975). Fotolytické.Ozařování vodného roztoku při 50 stupních po dobu 24 hodin vedlo k 23,06% výtěžku oxidu uhličitého (Knoevenagel a Himmelreich, 1976). Chemické/Fyzikální.Reakce ozonu v plynné fázi s pyridinem v syntetickém vzduchu při 23 stupních poskytla nitrovanou sůl mající vzorec: [C6H5NH]+NO3 - (Atkinson et al., 1987). Ozonizace pyridinu ve vodných roztocích při 25 stupních byla studována s a bez přidání terc-butylalkoholu (20 mM) jako lapače radikálů. S terc-butylalkoholem poskytla ozonizace pyridinu hlavně pyridin N-oxid (80% výtěžek), který byl velmi stabilní vůči ozonu. Bez terc-butylalkoholu se heterocyklický kruh rychle štěpí za vzniku amoniaku, dusičnanu a amidové sloučeniny N-formyloxamové kyseliny (Andreozzi et al., 1991). |
| Metabolismus | Pyridin je absorbován gastrointestinálním traktem, kůží a plícemi a je eliminován močí, stolicí, kůží a plícemi, a to jak jako metabolity, tak jako mateřská sloučenina (Jori et al 1983). Absorpce tkáněmi se zvyšuje s dávkou a eliminace je dvoufázové povahy (Zharikov a Titov 1982; HSDB 1988). Eliminace je rychlá a zdá se, že nedochází k žádné akumulaci tkáně (Jori et al 1983). His (1887) pozorování vylučování Af-methylpyridinu močí zvířaty, kterým byl podáván pyridin, bylo prvním příkladem Af-methylace. Mezi známé močové metabolity pyridinu u savců nyní patří pyridin N-oxid, N-methyl pyridin, 4-pyridon, 2-pyridon a 3-hydroxypyridin. Některé metabolity stále zbývá identifikovat (Damani et al 1982). Relativní množství metabolitů je vysoce závislé na druhu a dávce (Gorrod a Damani 1980). Například bylo prokázáno, že potkan vyloučí 70 % z dávky 1 mg/kg močí během prvních 24 hodin po podání dávky, ale toto číslo klesá pouze na 5,8 % u dávky 500 mg/kg (D'Souza et al 1980). Ačkoli se vylučování pyridinu a jeho metabolitů močí zdá být hlavní cestou eliminace, vylučování mimo moč nebylo rozsáhle studováno (Santodonato et al 1985). U králíků se ukázalo, že aktivita pyridin N-methyltransferázy je nejvyšší v plicním cytosolu a bylo zjištěno, že využívá 5-adenosylmethionin jako donor methylu (Damani et al 1986). Tato cesta je saturovatelná jak u potkana, tak u morčete (D'Souza et al 1980). Produkt této reakce, N-methyl pyridin, je méně chronicky toxický, ale akutněji toxický než pyridin (Williams 1959). Pyridin N-oxid je produkován systémem cytochromu P-450 a aktivita je indukována předúpravou fenobarbitalem nebo pyridinem, nikoli však {3-methylcholanthrenem (Gorrod a Damani 1979; Kaul a Novak 1987). U králíka alkoholem indukovatelný (a pyridinem indukovatelný) P-450 LM3Ase zdá být nízké Kmisozym, který katalyzuje produkci pyridinu Af-oxidu (Kim a Novak 1989). N-oxidace pyridinu může představovat cestu pro bioaktivaci (Santodonato et al 1985) a tato cesta se stává důležitější, když se dávka pyridinu zvyšuje (Damani et al 1982). |
| úložný prostor | Pyridin by měl být používán pouze v prostorách bez zdrojů vznícení a množství větší než 1 litr by mělo být skladováno v těsně uzavřených kovových nádobách v prostorách oddělených od oxidačních činidel. |
| Lodní doprava | UN1992 Hořlavé kapaliny, toxické, ne, třída nebezpečnosti: 3; Štítky: 3-Hořlavá kapalina, 6.1-Jedovaté materiály, je vyžadován technický název. |
| Způsoby čištění | Pravděpodobnými nečistotami jsou H2O a aminy, jako jsou pikoliny a lutidiny. Pyridin je hygroskopický a je mísitelný s H2O a organickými rozpouštědly. Může se sušit pevným KOH, NaOH, CaO, BaO nebo sodíkem s následnou frakční destilací. Další způsoby sušení zahrnují stání na molekulárních sítech Linde typ 4A, CaH2 nebo LiAlH4, azeotropní destilaci H2O s toluenem nebo *benzenem nebo zpracování s fenylmagnesiumbromidem v etheru s následným odpařením etheru a destilací pyridinu. Doporučená metoda [Lindauer Mukherjee Pure Appl Chem 27 267 1971] suší pyridin nad pevným KOH (20 g/kg) po dobu 2 týdnů a frakčně destiluje supernatant přes molekulární síta Linde typ 5A a pevný KOH. Produkt je skladován v dusíku bez CO{10}}. Pyridin lze skladovat v kontaktu s BaO, CaH2 nebo molekulovými síty. Nezásadité materiály lze odstranit destilací s vodní párou roztoku obsahujícího 1,2 ekvivalentu 20 % H2S04 nebo 17 % HCl, dokud se asi 10 % báze nepřenese spolu s nezásaditými nečistotami. Zbytek se poté zalkalizuje a báze se oddělí, vysuší NaOH a frakčně destiluje. Alternativně může být pyridin zpracován oxidačními činidly. Takto byl pyridin (800 ml) míchán po dobu 24 hodin se směsí síranu ceričitého (20 g) a bezvodého K2C03 (15 g), poté zfiltrován a frakčně destilován. Hurd a Simon [J Am Chem Soc 84 4519 1962] míchali pyridin (135 ml), vodu (2,5 1) a KMn04 (90 g) po dobu 2 hodin při 100 °C, poté stáli 15 hodin před odfiltrováním vysrážených oxidů manganu. Přidání pevného KOH (cca 500 g) způsobilo oddělení pyridinu. Byl dekantován, refluxován s CaO po dobu 3 hodin a destilován. Oddělení pyridinu od některých jeho homologů lze dosáhnout krystalizací oxalátů. Pyridin se vysráží ve formě oxalátu přidáním k míchanému roztoku kyseliny šťavelové v acetonu. Sraženina se odfiltruje, promyje se studeným acetonem a pyridin se regeneruje a izoluje. Jiné metody jsou založeny na tvorbě komplexů se ZnCl2 nebo HgCl2. |
| Nekompatibility | Prudká reakce se silnými oxidačními činidly; silné kyseliny; kyselina chlorsulfonová; anhydrid kyseliny maleinové; oleum jód. |
| Nakládání s odpady | Řízené spalování, při kterém jsou oxidy dusíku odstraňovány z odpadního plynu pračkou, katalytickými nebo tepelnými zařízeními. |
| Produkty a suroviny na přípravu pyridinu |
| Suroviny | Sulfuric acid-->Ammonia-->Benzene-->COAL TAR-->3-Picoline-->COKEOVENGAS-->1,5-DIHYDROCHLORID DIAMINOPENTANU |
| Přípravné produkty | Methyl 2-Fluoroisonicotinate-->2-ACETYL-5-CYANOTHIOPHENE-->5-BROMO-2-FLUOROCINNAMIC ACID-->4-NITROISOPHTHALIC ACID-->3,5-DIMETHOXYCINNAMIC ACID-->2-(2-Butoxyethoxy)ethyl acetate-->2,4-MESITYLENEDISULFONYL DICHLORIDE-->(4-FLUORO-BENZYL)-METHYL-AMINE-->1-Phenacylpyridinium bromide-->3-(TRIFLUOROMETHOXY)CINNAMIC ACID-->trans-Ferulic acid-->3-(Trifluoromethyl)pyrazole-->4-Fluorocinnamic acid-->Indigosol Green Blue IBC-->2-Amino-4-methyl-5-acetylthiazole-->Benzyl 2-chloroacetate-->5-ACETAMIDONICOTINIC ACID-->7-ACETOXYCOUMARIN-->2-AMINO-4-METHYL-QUINOLINE-3-CARBONITRILE-->N-PHENYLISONICOTINAMIDE-->Allyl methyl carbonate-->Pyridine-3-sulfonyl chloride hydrochloride-->Syringaldehyde-->2,4,5,6-TETRAMETHYLBENZENEDISULFONYL DICHLORIDE-->3-(3-METHYL-2-THIENYL)ACRYLIC ACID-->Vat Grey M-->17beta-Hydroxy-17-methylandrosta-4,9(11)-dien-3-one-->butyl N-phenylcarbamate-->3-Methoxycinnamic acid-->1-CHLORO-2-METHYLPROPYL CHLOROFORMATE-->Pyrazinecarbonitrile-->2-AMINO-6-CHLORO-3,5-DICYANOPYRIDINE-->4-BROMO-TETRAHYDROPYRAN-->Phenylcarbamic acid propyl ester-->Hydrocortisone acetate-->5-METHYLPICOLINIC ACID-->4-Acetamido-2-chloropyridine-->Pyridinium p-Toluenesulfonate-->1,2,4-Triazolo[4,3-a]pyridin-3(2H)-one-->Paraquat dichlorid |
Populární Tagy: pyridin, Čína výrobci pyridinu, dodavatelé, továrna
Mohlo by se Vám také líbit
Odeslat dotaz







